-
Numero contenuti
15663 -
Iscritto
-
Ultima visita
Tipo di contenuto
Profili
Forum
Orchidee
Diventa Socio
Calendario
Tutti i contenuti di Archivio Micologico
-

Pholiota adiposa (Batsch : Fr) P. Kumm. 1871
Archivio Micologico ha postato un topic nell'area Funghi Non Commestibili o Sospetti
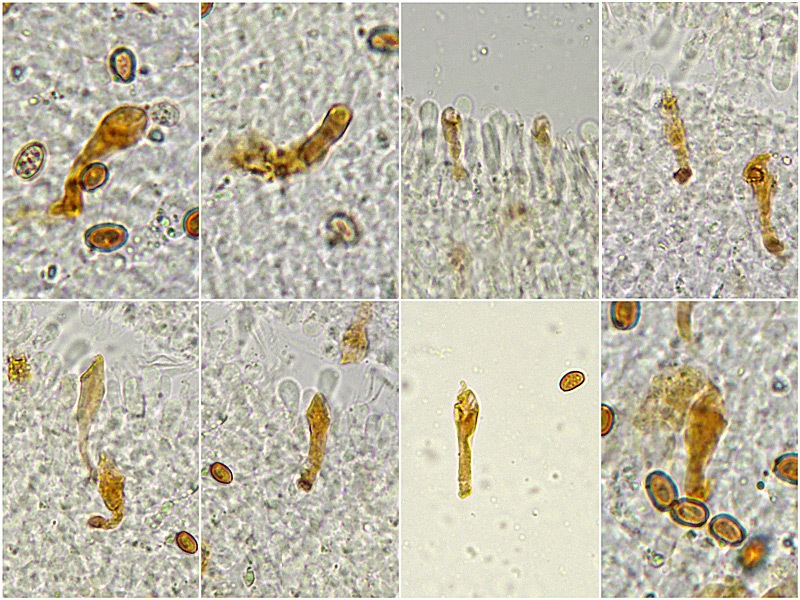
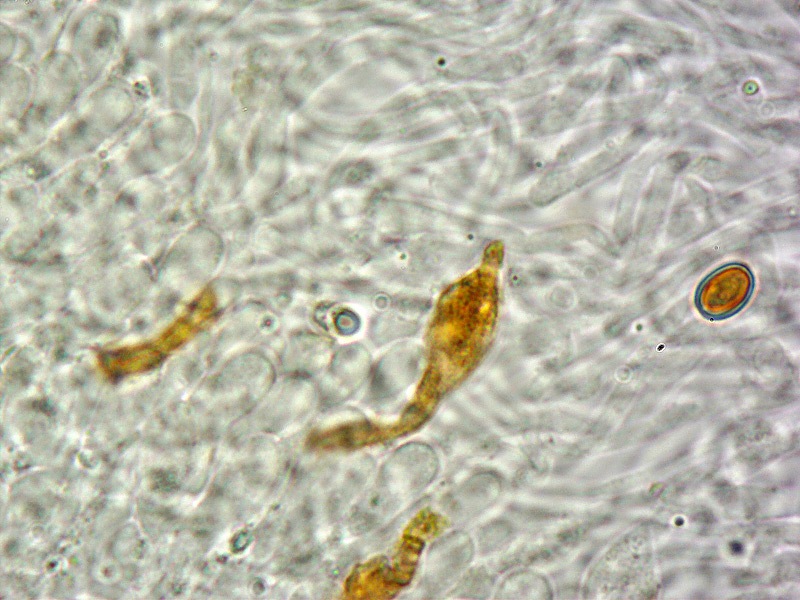
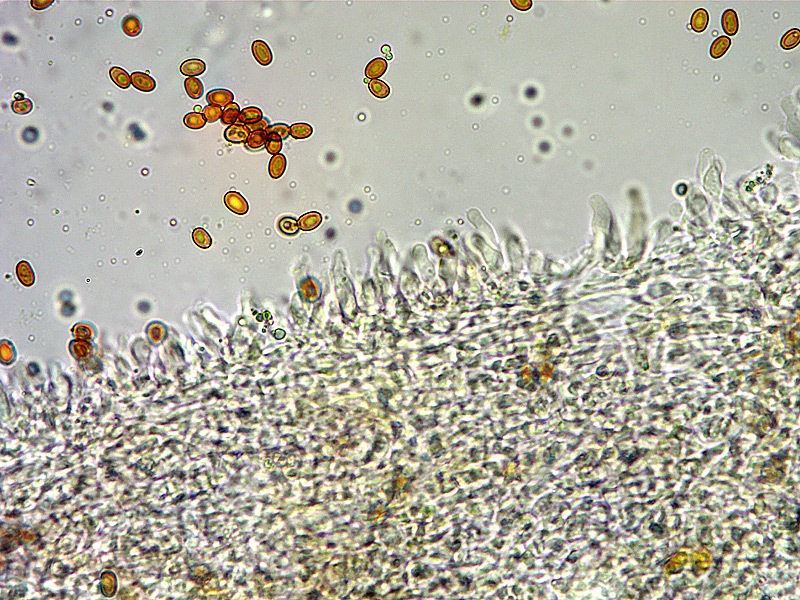
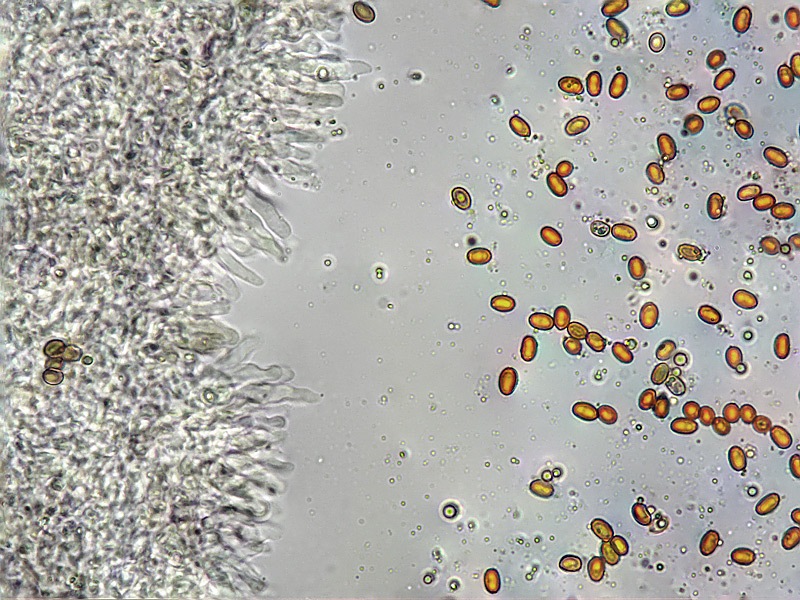
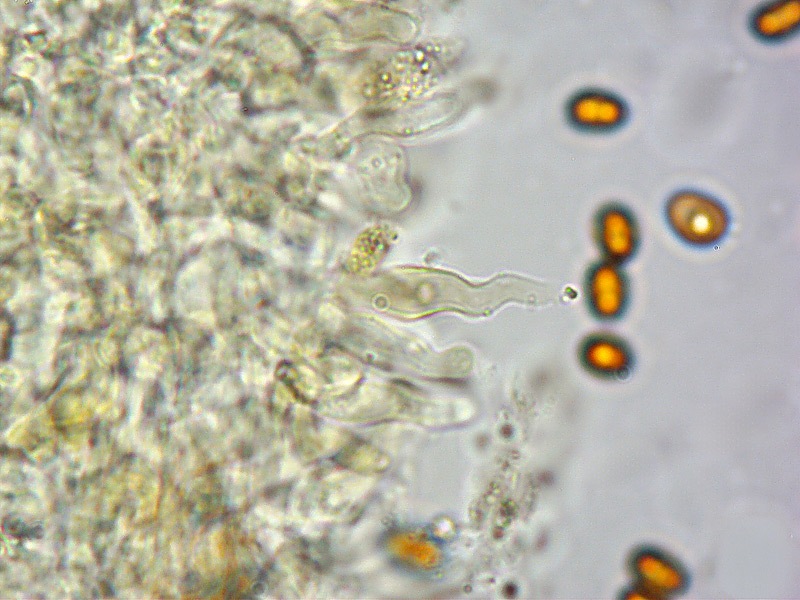
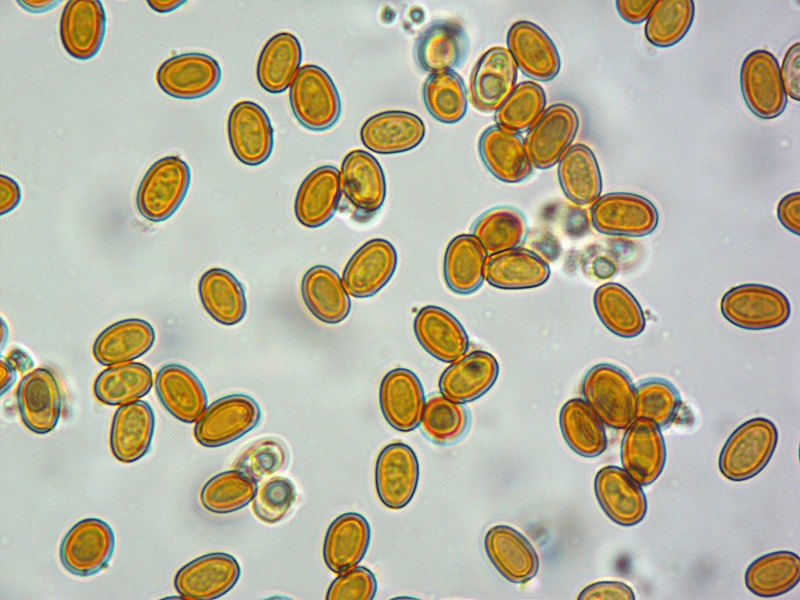
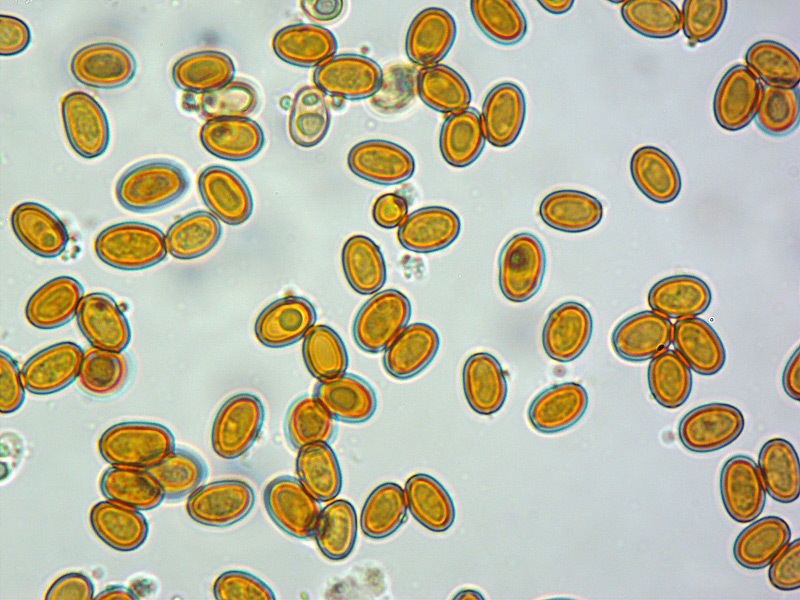
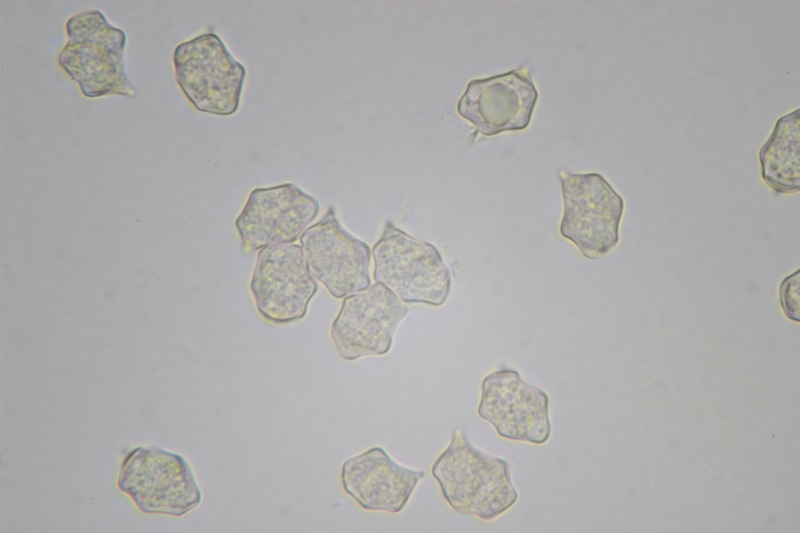
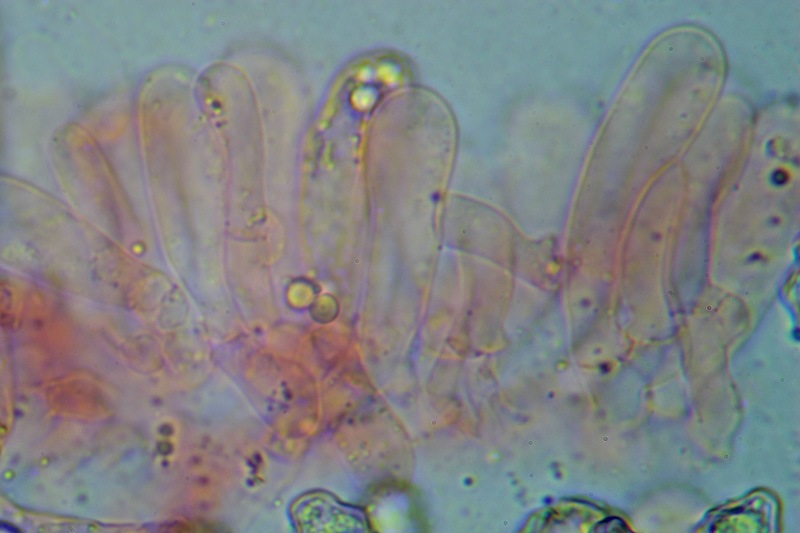
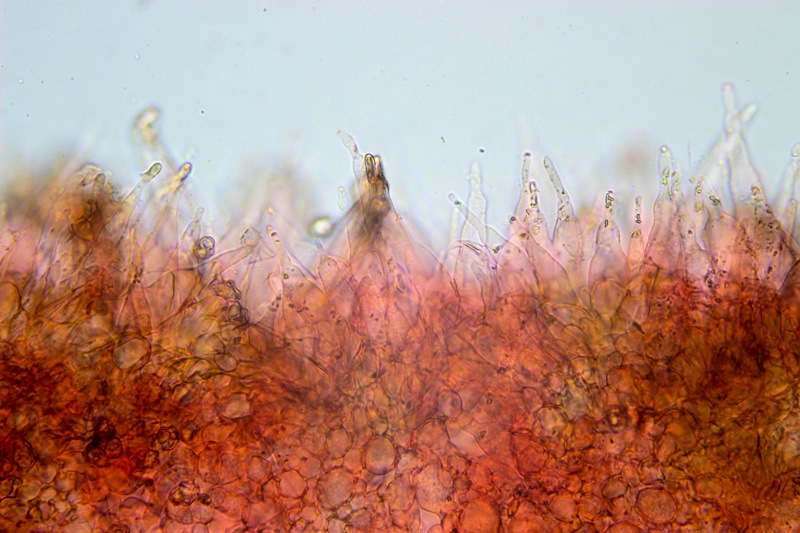
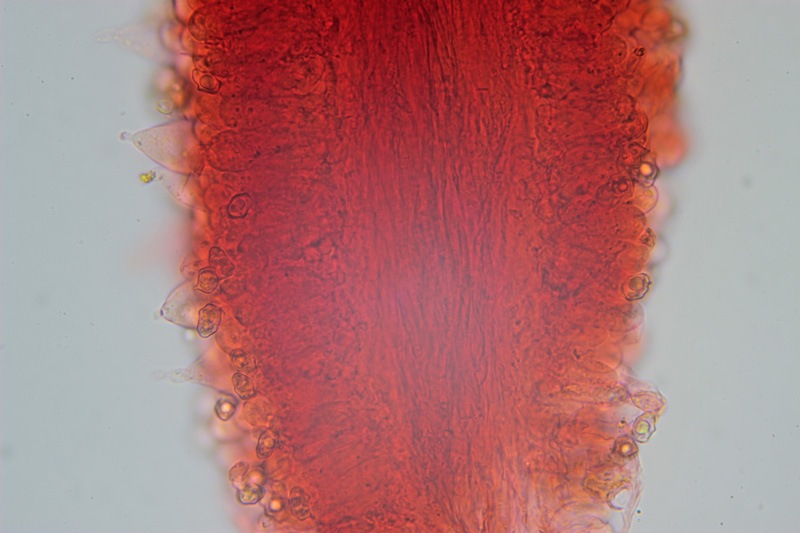
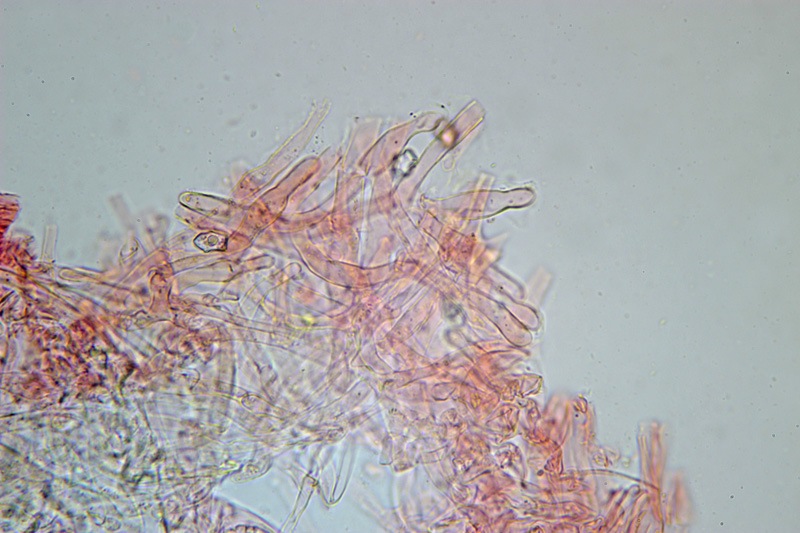
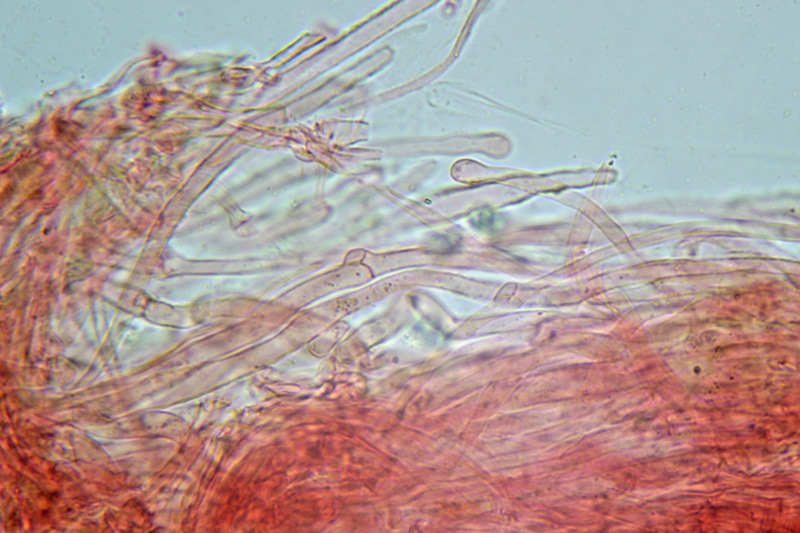
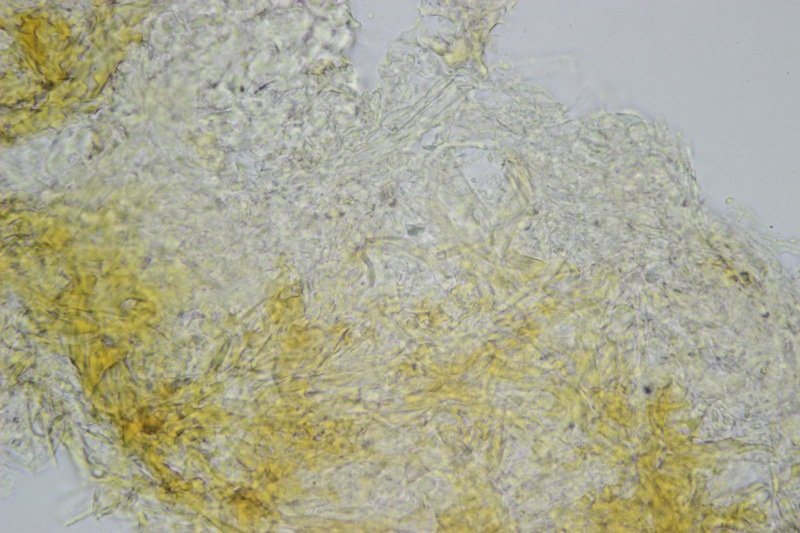
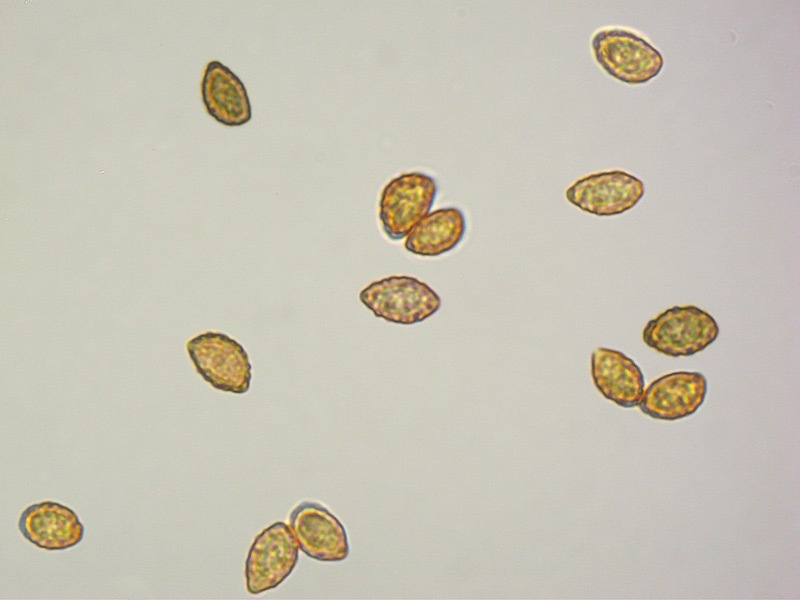
Pholiota adiposa (Batsch : Fr) P. Kumm. 1871 Tassonomia Divisione Basidiomycota Classe Agaricomycetes Ordine Agaricales Famiglia Strophariaceae Sinonimi Pholiota lilacifolia P.D. Orton 1976 Pholiota aurivella var. abietis-nordmanniana Singer 1930 Note tassonomiche Alcuni autori (AA.VV. 2012) ritengono questa specie sinonimo prioritario di Pholita aurivella (Batsch : Fr.) P. Kumm. s. auct p.p., sinonimia non condivisa da tutti gli autori. Etimologia L'epiteto Pholiota dal greco φολίς [pholís] = squama e da οὖς [otós] = orecchio, per la presenza di squame sul carpoforo. L'epiteto adiposa deriva dal latino ădeps = grasso, per la superficie del cappello viscida. Cappello 20-150 mm, emisferico, più disteso a maturità, con il margine involuto, presenta una cuticola, viscida, appiccicosa, di color giallo oro, poi bruno aranciato, con presenza di squame di colore marrone rossastro, non particolarmente rialzate, non echinulate. Imenoforo Lamelle mediamente fitte, da adnate a subdecorrenti, alternate a lemellule di varie dimensioni, inizialmente di colore crema ocracee, il filo lamellare è finemente fimbriato e sterile per la presenza di cheilocistidi, discolore rispetto alle facce lamellari. Anello Evidente, bianco, fibroso, membranaceo, ben evidente già nei soggetti molto giovani, spesso lembi abbondanti del velo secondario rimangono attaccati al bordo del cappello. Gambo Cilindrico, appuntito e spesso curvo alla base, squamoso su tutta la superficie inferiore all'anello. Carne Giallastra, odore insignificante, fungino; sapore neutro. Habitat Cespitoso, fruttifica su legno soprattutto di Fagus sylvatica, raramente su legno di conifere. Microscopia Cheilocistidi di profilo vario, ma non capitulati: strettamente clavati, lageniformi, serpeggianti. Pleurocrisocistidi spesso con forme irregolari, a volte muniti di una protuberanza apicale (mucronati), distribuiti nella trama lamellare. Basidi tetrasporici, clavati. Spore (6,9) 7,9-8,7 (9,7) × (4,8) 5,1-6,0 (6,6) µm; Q = (1,3) 1,4-1,6 (1,7); N = 50; Media = 8,3 × 5,5 µm; Qm = 1,5; ellissoidali, lisce a parete spessa, provviste di un evidente poro germinativo. GAF abbondanti, presenti in tutti i tessuti. Commestibilità e tossicità Non commestibile. Specie simili Pholiotha adiposa si caratterizza per la presenza di squame marroni sul cappello, presenza di cheilocistidi, pleurocrisocistidi, e per le spore con misure medie maggiori di 7 × 5 µm. Pholiota cerifera (P. Karst) P. Karst è la specie più simile a Pholiota adiposa, si distingue per il cappello non fortemente glutinoso, i chilocistidi clavati, ma più larghi di quelli di Pholiota adiposa e i crisocistidi abbondanti. Pholiota limonella (Peck) Sacc. è difficilmente distinguibile dal punto di vista dei caratteri macroscopici da Pholiota adiposa. Cresce su conifere e latifoglie ma difficilmente su Fagus sylvatica, ha spore più strette (4,0-5,2 (5,5) µm) di Pholiota adiposa ((4,5) 5,0-6,2 (6,5) µm). Pholiota jahnii Tjallingii-Beukers & Bas si distingue per le squame più appuntite e nerastre sul cappello, per le spore ellissoidali, ovoidali, più piccole (5-7 × 3-4 µm). Pholiota squarrosoides (Peck) Sacc. si distingue per le spore ellissoidali, faseoliformi in vista laterale, più piccole (4,5-6,5 × 2,5-3,5 µm). Pholiota lundbergii Jacobsson ha crescita terricola e spore più piccole (5,5-7,5 × 3,5-4,3 µm). Bibliografia AA.VV., 2012. Funga Nordica. Agaricoid, boletoid and cyphelloid genera. Ed. Nordsvamp. HOLEC, J., 2001. The Genus Pholiota in central and western Europe. Libri Botanici N° 2. Scheda di proprietà AMINT realizzata da Tomaso Lezzi - Approvata e Revisionata dal CLR Micologico di AMINT. Regione Lazio. Maggio 2026. Foto di Tomaso Lezzi. Crisocistidi. Osservazione in KOH, a 600×. Crisocistidio. Osservazione in KOH, a 1000×. Cheilocistidi. Osservazione in KOH, a 400×. Crisocistidi. Osservazione in KOH, a 1000×. Spore. Osservazione in KOH, a 1000×. -

Conioexocarpus cretaceus (Bull.) R.L. Zhao & J.X. Li 2025
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Conioexocarpus cretaceus (Bull.) R.L. Zhao & J.X. Li 2025. Spagna. Settembre 2025. Foto di Tomaso Lezzi. Ritrovamento effettuato all'interno del "Jardí Botànic de Barcelona" (Giardino Botanico di Barcellona). -

Conioexocarpus cretaceus (Bull.) R.L. Zhao & J.X. Li 2025
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Conioexocarpus cretaceus (Bull.) R.L. Zhao & J.X. Li 2025. Regione Lazio. Settembre 2025. Foto di Tomaso Lezzi. Ritrovamento effettuato in un vaso di orchidee in casa. -

Geopora sumneriana (Cooke ex W. Phillips) M. Torre 1976
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Geopora sumneriana (Cooke ex W. Phillips) M. Torre. Regione Umbria. Marzo 2026. Foto di Tomaso Lezzi. Ritrovamento sotto Cedrus atlantica.- 30 risposte
-
- geopora sumneriana
- sepultaria sumneriana
- (e 1 in più)
-

Agaricus menieri Bon 1981
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Velenosi
Agaricus menieri Bon. Regione Lazio. Marzo 2026. Foto Tomaso Lezzi. Ritrovamento effettuato a 50 metri dalla spiaggia, su terreno sabbioso, sotto Pinus pinea, Quercus suber, Quercus ilex e Cistus salviaefolius. Anello doppio, sezione con base che vira al giallo. Sezione con base che vira al giallo. -

Hygrophorus marzuolus (Fr. : Fr.) Bres. 1893
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Commestibili
-

Cortinarius caligatus Malençon 1970
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Cortinarius caligatus Malençon. Regione Lazio. Novembre 2025. Foto di Tomaso Lezzi. Raduno AMER 2025 a Sabaudia Ritrovamento sotto sughera. KOH negativo sulla cuticola. -

Cortinarius cingulatus (Velen.) Rob. Henry 1945
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
-

Agaricus depauperatus (F.H. Møller) Pilát 1951
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Commestibili
Agaricus depauperatus (F.H.Møller) Pilát. Regione Lombardia. Ottobre 2022. Foto Massimo Biraghi. -

Pholiota limonella (Peck) Sacc. 1887
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Pholiota limonella (Peck) Sacc. Regione Lombardia, Val Brembana, loc. Ornica. Settembre 2015. Foto di Massimo Biraghi. -

Entoloma excentricum Bres. 1881
Archivio Micologico ha postato un topic nell'area Funghi Non Commestibili o Sospetti
Entoloma excentricum Bres. 1881 Tassonomia Divisione Basidiomycota Classe Agaricomycetes Ordine Agaricales Famiglia Entolomataceae Cappello Cappello circa 40-50 mm, non igrofano e non striato, al momento della raccolta con delle fiammature giallo ocra in superficie. Lamelle Lamelle con il filo eterogeneo un poco più scuro. Gambo Gambo 30-70 × 4-7 mm. Carne Tutte le superfici imbrunenti per invecchiamento; odore non distintivo, non di farina, sapore mite, appena un accenno di pizzicore sulla punta della lingua, ma dopo un po' di tempo. Microscopia Pileipellis una cutis di ife gelificate, con GAF, gli elementi terminali in alcuni casi nella forma ricordano i cistidi imeniali ma più piccoli e stretti. Pigmenti. In tutti i preparati si nota un pigmento intercellulare grossolano, inizialmente giallo ma poi sempre più scuro. Spore 11,5-13 × 8,3-9,4 µm; Q = 1,2-1,5; eterodiametriche. Basidi tetrasporici con GAF alla base. Cistidi imeniali lageniformi-fusiformi molto grandi sporgenti dal filo e dalle facce delle lamelle. Caulocutis non osservata. Habitat Bosco di latifoglia, con crescita gregaria nel sottobosco. Osservazioni L'exsiccatum diventa bruno nerastro. Regione Lombardia. Ottobre 2020. Foto di Sergio Mombrini. Spore 11,5-13 × 8,3-9,4 µm; Q = 1,2-1,5; eterodiametriche. Osservazione in acqua, a 1000×. Basidi tetrasporici con GAF alla base. Osservazione in rosso Congo, a 1000×. Cheilocistidi sporgenti dal filo lamella. Osservazione in rosso Congo, a 400×. Lamella sezione longitudinale, Pleurocistidi sporgenti. Osservazione in rosso Congo, a 400×. Epicutis, alcuni elementi terminali cistidiformi. Osservazione in rosso Congo, a 400×. Epicutis, ife con GAF. Osservazione in rosso Congo, a 400×. Epicutis, pigmento intercellulare grossolano. Osservazione in acqua, a 400×. -

Leucoagaricus subvolvatus (Malençon & Bertault) Bon 1977
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Leucoagaricus subvolvatus (Malençon & Bertault) Bon. Regione Puglia, Bosco Isola, Parco Nazionale del Gargano. Dicembre 2018. Foto di Raffaele Mininno. Questa specie si riconosce per la crescita prevalentemente sabulicola, per la base del gambo che simula una volva in virtù della presenza di un bulbo nettamente marginato, per il cappello biancastro con il disco umbonato molto scuro. -

Pholiota limonella (Peck) Sacc. 1887
Archivio Micologico ha postato un topic nell'area Funghi Non Commestibili o Sospetti
Pholiota limonella (Peck) Sacc. 1887 Tassonomia Divisione Basidiomycota Classe Agaricomycetes Ordine Agaricales Famiglia Strophariaceae Regione Emilia Romagna. Ottobre 2022. Foto di Massimo Biraghi. N° Long. Larg. Q Moy 7,95 5,58 1,43 µm Min 7,20 4,94 1,28 µm Max 8,88 6,14 1,65 µm média 7,89 5,55 1,42 µm N= 30 ; (7,20) 7,43 - 7,88 - 8,72 (8,88) × (4,94) 5,24 - 5,55 - 5,95(6,14) µm Qm= 1,43. -

Pholiotina parvula (Døssing & Watling) Bon 1991
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Pholiotina parvula (Døssing & Watling) Bon. Regione Lombardia, Arcene, parco pubblico. Dicembre 2015. Foto e microscopia di Massimo Biraghi. Spore ellissoidali, con piccolo poro germinativo centrale. N° Long. Larg. Q Moy 6,70 3,72 1,81 Min 5,98 3,23 1,60 Max 7,94 4,32 1,94 Media 6,60 3,68 1,83 Cheilocistidi. Caulocistidi. Elementi della pileipellis. -

Sarcodon squamosus (Schaeff.) P. Karst. 1889
Archivio Micologico ha postato un topic nell'area Funghi Non Commestibili o Sospetti
Sarcodon squamosus (Schaeff.) P. Karst. 1889 Tassonomia Divisione Basidiomycota Classe Agaricomycetes Sottoclasse Holobasidiomycetidae Ordine Thelephorales Famiglia Bankeraceae Regione Liguria. Novembre 2015. Foto e descrizione di Massimo Biraghi. -

Urnula craterium (Schwein.) Fr. 1851
Archivio Micologico ha postato un topic nell'area Funghi Non Commestibili o Sospetti
Urnula craterium (Schwein.) Fr. 1851 Tassonomia Divisione Ascomycota Classe Pezizomycetes Ordine Pezizales Famiglia Sarcosomataceae Bibliografia CARBONE M. & AGNELLO C. 2010. Appunti di studio su Urnula hiemalis Nannf. Ascomycete.org, 4 (5): 99-108. Regione Friuli-Venezia Giulia, Prato Carnico (UD). Aprile 2014. Foto di Umberto Zanghi. Ritrovamento in un bosco misto con presenza di Abete, etc blablabla a 800 m s.l.m. -

Cortinarius sodagnitus Rob. Henry 1935
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Cortinarius sodagnitus Rob. Henry. Regione Toscana; Ottobre 2022; Foto e microscopia di Mario Iannotti. 1° CSM di M.te Rufeno e M.te Amiata – 22-26 Ottobre 2022 Cappello di colore lilla-azzurro, con sfumature ocracee e decolorazione al biancastro. Lamelle fitte, grigio-azzurro, poi grigio-brune. Gambo cilindrico, con sfumature blu-violette all'apice. Odore terroso. Reazione macrochimica con KOH sul cappello e sulla bulbipellis di un rosa laccato. Spore (8,9) 9,4-10,8 (11,0) × (5,6) 5,8-6,4 (6,6) µm; Q = (1,5) 1,6-1,7 (1,8); Media = 10,2 × 6,2 µm; Qm = 1,7; amigdaliformi, verrucose. Spore (8,9) 9,4-10,8 (11,0) × (5,6) 5,8-6,4 (6,6) µm; Q = (1,5) 1,6-1,7 (1,8); Media = 10,2 × 6,2 µm; Qm = 1,7; amigdaliformi, verrucose. Osservazione in rosso Congo ammoniacale, a 1000×. Foto di Tomaso Lezzi. In foto reazione rosso-rosa brillante con KOH su cappello e bulbo.- 1 risposta
-
- calonarius sodagnitus
- cortinarius provencalis
- (e 3 in più)
-

Melanoleuca strictipes (P. Karst.) Jul. Schäff. 1951
Archivio Micologico ha postato un topic nell'area Funghi Non Commestibili o Sospetti
Melanoleuca strictipes (P. Karst.) Jul. Schäff. 1951 Tassonomia Divisione Basidiomycota Classe Agaricomycetes Ordine Agaricales Famiglia Melanoleucaceae Genere Melanoleuca Sottogenere Urticocystis Etimologia L'epiteto Melanoleuca deriva dal greco: μέλας [mèlas] = nero, scuro e λευκός [leucòs] = bianco, cioè nero e bianco, per i colori contrastanti che spesso questo genere mostra tra cappello e gambo. Regione Trentino-Alto Adige (Provincia autonoma di Trento). Settembre 2013. Foto di Mario Iannotti. 3º Congresso trentino sui funghi alpini, Cles (TN), Loc. Malgaroi. Ritrovamento nell'esteso alpeggio della Val Nana, habitat prateria alpina, altitudine 2.100 m s.l.m., determinata macro e microscopicamente nel corso del convegno. -

Pseudosperma cupreum G.B. Galeotti, Rubini, Para, C. Riccioni & B. Belfiori 2025
Archivio Micologico ha postato un topic nell'area Funghi Velenosi
Pseudosperma cupreum G.B. Galeotti, Rubini, Para, C. Riccioni & B. Belfiori 2025 Tassonomia Divisione Basidiomycota Classe Agaricomycetes Ordine Agaricales Famiglia Inocybaceae Sezione Rimosae Etimologia L'epiteto Pseudosperma deriva dal prefisso greco ψευδής- [pseudes-] = falso e sperma dal greco σπέρμα [sperma] = seme, spora, nome creato quando sono stati separati filogeneticamente alcuni generi prima inclusi nel genere Inocybe. L'epiteto cupreum deriva dal latino cuprĕus = color del rame, per la tonalità ramata presente al centro del pileo, caratteristica della specie. Cappello Largo mediamente 20-40 mm, leggermente carnoso, inizialmente conico-campanulato, successivamente appiattito con un umbone prominente; margine regolare e involuto, a volte revoluto negli esemplari maturi. Cuticola rimosa,fibrillosa, secca, screpolata longitudinalmente, senza residui di velo. Colore di fondo da ocraceo a giallo chiaro, compatto con tonalità rosso-ramate al centro da cui si irradiano verso il margine filamenti filiformi dello stesso colore. Imenoforo A lamelle distanziate, da adnate a uncinate, strette, sottili e irregolari, con lamellule di dimensioni variabili, inizialmente biancastre, poi ocra, con sfumature olivacee e macchie color ruggine, infine brune a maturità. Il margine lamellare è ondulato, finemente eroso, sterile e più chiaro della faccia lamellare. Impronta sporale bruno-ocracea. Gambo Lungo 40-60 mm, centrale, cilindrico, a volte ricurvo alla base, bianco e pruinoso all'apice, con sfumature ocraceo-fulve vicino alla base e quando contuso, la base è generalmente clavata a volte nettamente bulbosa. Carne Contesto fibroso e sempre biancastro nel gambo, fragile nel cappello. Odore leggermente aromatico con componente spermatica. Habitat Vegetazione mista comprendente Alnus glutinosa (L.)., Populus alba (L.)., Salix sp., Acer spp. La specie fruttifica da tarda primavera, inizio estate, e si protrae per tutto il periodo autunnale (GALEOTTI 2025). Microscopia Spore (9,2) 9,7-11,2 (13,3) × (5,0) 5,3-6,4 (6,6) µm; Q = (1,5) 1,6-2,0 (2,3); N = 42; Media = 10,3 × 5,9 µm; Qm = 1,8 lisce e asimmetriche, ellissoidali in vista frontale e amigdaliformi in vista laterale, occasionalmente ovoidali e faseoliformi. Basidi prevalentemente tetrasporici, clavati e multiguttulati. Cheilocistidi (27,3) 29,6-43,4 (55,3) × (8,0) 8,8-15,7 (22,7) µm; Q = (2,3) 2,4-3,6 (3,9); N = 22; Media = 36,8 × 12,4 µm; Qm = 3,1; prevalentemente clavati alcuni cilindrici. Pleurocistidi assenti. Caulocistidi (21,2) 30,4-56,7 (61,7) × (5,8) 6,9-11,0 (12,2) µm; Q = (2,4) 3,0-6,5 (8,4); N = 18; Media = 42,3 × 9,1 µm; Qm = 4,8; osservati solo all'apice del gambo, altamente variabili, cilindrici, clavati, subcapitati, mucronati, lanceolati, settati, catenulati. Pileipellis formata da ife parallele, con la subpellis composta da ife più spesse e leggermente rigonfie; mostra pigmento parietale evidente, finemente incrostante. GAF presenti in tutti i tessuti osservati. Commestibilità e tossicità Non si conoscono le caratteristiche di commestibilità di questa specie recentemente scoperta, si ritiene velenosa come tutte le Inocybe, con sindrome muscarinica. Per approfondimenti consulta la Pagina di Micotossicologia. Specie simili Pseudosperma cupreum è morfologicamente simile a diverse specie del gruppo Pseudosperma rimosum sl., rendendo la sua differenziazione altamente impegnativa. I pochi tratti morfologici distintivi includono i toni ramati del pileo, un gambo spesso ingrossato o bulboso alla base, che tende a macchiarsi quando contuso, l'assenza di veli e la sua preferenza per un habitat ripariale. Tra le specie filogeneticamente correlate a P. cupreum, le più rappresentative sono elencate di seguito, insieme alle loro principali differenze: Pseudosperma umbrinellum (Bres.) Matheny & Esteve-Rav. si differenzia per il suo cappello da nocciola a marrone cannella e spore leggermente più lunghe (BRESDOLA 1905, LARSSON et al. 2009); Pseudosperma melliolens (Kühner) Matheny & Esteve-Rav. si differenzia per il pileo marrone, spore più grandi, odore mielato e habitat (CERVINI et al. 2020); Pseudosperma napaeanum Bandini & B. Oertel si differenzia per il colore del cappello, la presenza di cheilocistidi subcapitati, per le spore più grandi e la preferenza per gli ambienti alpini (BANDINI & OERTEL 2020) Pseudosperma guttuliferum (Kühner) Matheny & Esteve-Rav., si distingue per le spore più grandi e la preferenza per gli ambienti alpini (BANDINI & OERTEL 2020); Pseusosperma quercinum Naseer & Jabeen si differenzia per il colore del cappello, la base del gambo non bulbosa e ricurva, l'odore mielato e l'habitat sotto Quercus spp. (NASEER et al. 2023); Pseudosperma neoumbrinellum (T. Bau & Y.G. Fan) Matheny & Esteve-Rav. si differenzia per il pileo da marrone cioccolato a marrone scuro, giallo ocra sull'umbone (BAU & FAN 2018). Pseudosperma littorale (Pegler) Matheny & Esteve-Rav. ha un pileo giallo ambrato e cresce in un habitat diverso (PEGLER 1983); Pseudosperma fissuratum (Matheny & Bougher) Matheny & Esteve-Rav. si differenzia per la presenza di cheilocistidi subcapitati, l'odore non spermatico e l'habitat sotto Eucalyptus sp. (MATHENY & BOUGHER 2017). Altre specie simili, non strettamente correlate filogeneticamente ma comparabili a Pseudosperma cupreum includono: Pseudosperma ushae Bandini & G. Bandini la quale differisce per i toni arancio-rossastri, la presenza di minute fibrille sulla superficie del pileo, basidiospore più piccole e l'odore non spermatico (BANDINI et al. 2022); Pseudosperma fascinosum Bandini & B. Oertel la quale differisce per la presenza di una velipellis grigiastra e l'odore non spermatico (BANDINI et al. 2022); Pseudosperma squamatum (J.E. Lange) Matheny & Esteve-Rav. la quale si differenzia per il pileo giallo-fulvo con tipica presenza di squame scure appressate (LANGE 1917). Bibliografia BANDINI D. & OERTEL B. 2020. Three new species of the genus Pseudosperma (Inocybaceae). Czech Mycology 72: 221-250. https://doi.org/10.33585/cmy.72205 BANDINI D., OERTEL B. & EBERHARDT U. 2022. Noch mehr risspilze (3): einundzwanzig neue arten der familie inocybaceae. Mycologia Bavarica 22: 31–138. BAU T. & FAN Y.G. 2018. Three new species of Inocybe sect. Rimosae from China. Mycosystema 37: 693-702. BRESADOLA G. 1905. Hymenomycetes novi vel minus cogniti. Annales Mycologici 3: 161. CERVINI M., BIZIO E. & ALVARADO P. 2020. Quattro nuove specie italiane del genere Pseudosperma (Inocybaceae) con odore di miele. GALEOTTI G.B., RUBINI A., PARA R., RICCIONI C., BELFIORI B. 2025. Description of two new species of Pseudosperma in central Italy. Phytotaxa 693 (2): 12. https://phytotaxa.mapress.com/pt/article/view/phytotaxa.693.2.1 LANGE J.E. 1917. Studies in the Agarics of Denmark. Part III. Pluteus. Collybia. Inocybe. Dansk Botanisk Arkiv 2: 1–50. https://doi.org/10.1007/978-3-662-42454-4_10 LARSSON E., RYBERG M., MOREAU PA., DELCUSE MATHIESEN Å. & JACOBSSON S. 2009. Taxonomy and evolutionary relationships within species of section Rimosae (Inocybe) based on ITS, LSU and mtLSU sequence data. Persoonia 23: 86–98. https://doi.org/10.3767/003158509X475913 MATHENY P.B. & BOUGHER N.L. 2017. Fungi of Australia: Inocybaceae. CSIRO Publishing. MATHENY PB, HOBBS A.M. & ESTEVE-RAVENTÓS F. 2020 Genera of Inocybaceae: New skin for the old ceremony. Mycologia 112: 83–120. https://doi.org/10.1080/00275514.2019.1668906 NASEER A., JABEEN S. ASHFAQ A., AKBAR M., HUSSAIN S.I. & KHALID A.N. 2023. Pseudosperma quercinum sp. nov. (Inocybaceae) from the Himalayan forests of Pakistan. Phytotaxa 622: 260–270. https://doi.org/10.11646/phytotaxa.622.4.3 PEGLER D.N. 1983. Agaric Flora of the Lesser Antilles. Kew Bulletin, Additional Series 9: 1-668. Scheda di proprietà AMINT realizzata da Giovanni Galeotti - Approvata e Revisionata dal CLR Micologico di AMINT. Regione Umbria. Luglio 2025. Foto di Giovanni Galeotti. Foto in habitat con le principali essenze arboree presenti. Gli esemplari sono stati raccolti nei mesi di Luglio-Agosto 2025 e altre raccolte pubblicate nell'articolo originale, sono state effettuate a fine giugno, ottobre e novembre, tutte i campioni provengono da un ecosistema ripariale, situato nella pianura alluvionale formata dal fiume Tevere, a 280 m di altitudine, caratterizzato da un suolo sabbioso-limoso (pH = 7,5), frequentemente soggetto ad allagamenti durante la stagione delle piogge, e da una vegetazione mista comprendente Alnus glutinosa (L.)., Populus alba (L.)., Salix sp., Acer spp. Agosto 2025. Foto e microscopia di Giovanni Galeotti. Raccolta del 2 Agosto 2025. (Exsiccatum GG0075) Cheilocistidi. Osservazione in rosso Congo, a 100×. Cheilocistidi. Osservazione in rosso Congo, a 400×. Cheilocistidi. Osservazione in rosso Congo, a 1000×. Basidi. Osservazione in rosso Congo, a 1000×. Caulocistidi. Osservazione in rosso Congo, a 400×. Caulocistidi. Osservazione in rosso Congo, a 1000×. Caulocistidi e GAF. Osservazione in rosso Congo, a 1000×. Spore. Osservazione in acqua, a 1000×. -

Pholiota conissans (Fr.) Kuyper & Tjall.-Beuk. 1986
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Pholiota conissans (Fr.) Kuyper & Tjall.-Beuk. Regione Umbria. Novembre 2022. Foto di Mario Iannotti. Stazione consolidata al teatro romano di Città di Castello e verificata microscopicamente.- 1 risposta
-
- pholiota conissans
- pholiota graminis
- (e 3 in più)
-

Pholiota conissans (Fr.) Kuyper & Tjall.-Beuk. 1986
Archivio Micologico ha postato un topic nell'area Funghi Non Commestibili o Sospetti
Pholiota conissans (Fr.) Kuyper & Tjall.-Beuk. 1986 Tassonomia Divisione Basidiomycota Classe Agaricomycetes Ordine Agaricales Famiglia Strophariaceae Sinonimi Pholiota inaurata (W.G. Sm.) M.M. Moser, 1953 Pholiota graminis (Quél.) Singer, 1951 Dryophila conissans (Fr.) Quél. 1886 Flammula conissans (Fr.) Gillet, 1838 Note tassonomiche Pholiota conissans è un complesso di specie che appartengono al sottogenere Pholiota, sezione Gummosae Jacobsson. Etimologia L'epiteto Pholiota dal greco φολίς [pholís] = squama e da οὖς [otós] = orecchio, per la presenza di squame sul carpoforo. L'epiteto conissans deriva dal greco κονίζω [conío] = cospargo di polvere, per l'abbondante sporata che genera a maturazione. Cappello Di taglia medio piccola 20-50 mm, emisferico nei giovani soggetti poi disteso, con il margine intero a lungo involuto, presenta una cuticola liscia, viscida e untuosa con l'umidità, asciutta a maturità, giallo-ocracea, con presenza di guttule oleose sparse in corrispondenza del margine, al disco è spesso evidente un largo umbrone schiacciato, con colori intensi e sfumature rossastre. Imenoforo Lamelle mediamente fitte, da adnate a subdecorrenti, alternate a lemellule di varie dimensioni, inizialmente di colore crema ocracee, poi bruno rossastre, il filo lamellare è finemente fimbriato e sterile per la presenza di abbondanti cheilocistidi, discolore rispetto alle facce lamellari. Anello Evidente nei soggetti molto giovani, cortiniforme, si presenta filamentoso e vischioso a tempo umido, residua un cercine discolore nei soggetti adulti nella parte alta del gambo, fino a svanire totalmente a maturazione. Gambo Cilindrico, sinuoso, spesso ricurvo, allargato all'inserzione con le lamelle, attenuato verso la base, di colore bianco giallastro e pruinoso sopra la zona anulare, giallastro e decorato da sottili squame per la maggior parte della lunghezza, rossastro con squame maggiormente evidenti alla base. Carne Giallastra, fibrosa, tendente a scurire alla base del gambo, odore insignificante, sapore inizialmente dolciastro poi amarognolo. Habitat Fruttifica in luoghi umidi in presenza di Graminaceae, su detriti organici di Typha angusitifolia, Cyperus papyrus e Salix spp. Microscopia Pileipellis formata da una ixocutis con ife rialzate immerse in uno strato di gel che tende a formare un ixotricoderma, e uno strato sottostante di ife parallele più grandi e molto allungate. Cheilocistidi molto abbondanti, cilindrici, lageniformi, con apice capitulato, ialini, a parete sottile. Crisocistidi rari, alternati ai cheilocistidi. Crisopleurocistidi fusiformi e clavati, spesso con apice mucronato, con granuli interni giallastri e altamente rifrangenti. Basidi tetrasporici, clavati. Spore (6,4) 6,7-7,4 (7,7) × (3,4) 3,7-4,1 (4,2) µm; Q = (1,6) 1,7-2,0 (2,2); N = 42; Media = 7,0 × 3,8 µm; Qm = 1,8; ellissoidali in vista frontale, leggermente faseoliformi in vista laterale, provviste di un piccolo ma evidente poro germinativo. GAF abbondanti, presenti in tutti i tessuti. Commestibilità e tossicità Non commestibile. Specie simili Pholiota conissans si caratterizza per l'habitat di Graminaceae e piante palustri, per il cappello molto viscido e per le guttule presenti sul cappello stesso. Pholiota pityrodes (F. Brig.) Holec differisce per carpofori di taglia molto minuta (0,5-2,3 cm), spore piccole (5,0-7,0 × 2,5-3,0 (-3,5) µm), e per i cheiloleptocistidi da lageniformi a subcapitulati. Pholiota gummosa (Lasch) Singer ha pileo squamoso, colori colori giallo-olivastri, giallo-verdastri, cheiloleptocistidi da clavati a lageniformi misti a pochi subcapitulati e habitat diverso. Bibliografia AA.VV., 2012. Funga Nordica. Agaricoid, boletoid and cyphelloid genera. Ed. Nordsvamp. UZUNOV B.A. 2017. First record of Marasmius limosus and Pholiota conissans (Basidiomycota) in Bulgaria. GSU.BIOFAC.Bot. 100: 62-66. HOLEC, J., 2001. The Genus Pholiota in central and western Europe. Libri Botanici N° 2. Scheda di proprietà AMINT realizzata da Giovanni Galeotti - Approvata e revisionata dal CLR Micologico di AMINT. Regione Umbria; Ottobre 2022. Foto e microscopia di Giovanni Galeotti. (Exsiccatum -GG281022-01) Luogo del ritrovamento situato su scavi archeologici, che hanno portato alla luce i resti di un anfiteatro romano, in una zona umida e paludosa, oggi prato di graminacee e trifoglio costituito da terreno di riporto, fino ad un paio di anni fa nello stesso punto, era presente un canneto di Typha angusitifolia che ancora a tratti riemerge; sui detriti di queste piante in decomposizione si è sviluppata una consistente colonia di questi funghi. Carpofori fascicolati, raramente si osservano soggetti singoli. Soggetti adulti con squame rossastre alla base del gambo. Cheilocistidi. Osservazione in rosso Congo, a 400×. Cheilocistidi. Osservazione in rosso Congo, a 1000×. Pleurocrisocistidi. Osservazione in rosso Congo, a 1000×. Basidi. Osservazione in rosso Congo, a 1000×. Pileipellis. Osservazione in rosso Congo, a 400×. Pileipellis. Osservazione in rosso Congo, a 1000×. GAF. Osservazione in rosso Congo, a 400×. GAF. Osservazione in rosso Congo, a 1000×. Spore (6,4) 6,7-7,4 (7,7) × (3,4) 3,7-4,1 (4,2) µm; Q = (1,6) 1,7-2,0 (2,2); N = 42; Media = 7,0 × 3,8 µm; Qm = 1,8; ellissoidali in vista frontale, leggermente faseoliformi in vista laterale, provviste di un piccolo ma evidente poro germinativo. Osservazione in acqua, a 1000×.- 1 risposta
-
- pholiota conissans
- pholiota graminis
- (e 3 in più)
-

Cortinarius viridicoeruleus Chevassut & Rob. Henry 1975
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Cortinarius viridicoeruleus Chevassut & Rob. Henry. Regione Toscana. Ottobre 2022. Foto di Tomaso Lezzi. 1° CSM di M.te Rufeno e M.te Amiata – 22-26 Ottobre 2022- 2 risposte
-
- cortinarius viridicoeruleus
- phlegmacium lepistoides
- (e 1 in più)
-

Chalciporus piperatus (Bull. : Fr.) Bataille 1908
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Chalciporus piperatus (Bull. : Fr.) Bataille. Regione Trentino. Settembre 2013. Foto di Tomaso Lezzi 3º Congresso trentino sui funghi alpini, Cles (TN), Loc. Malgaroi. Un particolare dei pori color cannella. -

Cortinarius caroviolaceus P.D. Orton 1960
Archivio Micologico ha risposto alla discussione di Archivio Micologico in Funghi Non Commestibili o Sospetti
Cortinarius caroviolaceus P.D. Orton. Regione Abruzzi. Ottobre 2024. Foto di Tomaso Lezzi. Spore. Osservazione in KOH, a 1000×.


-03.jpg.1354008db92101376ecb4cffa4be42e5.jpg)
-04.jpg.e76d9665cc708b8a6b7a8254f1a9d8ef.jpg)
-05.jpg.18654a2e5855af15482170b369a66507.jpg)